Különbség Valency és Valence Electrons | Valency vs Valence Electrons
Kulcsváltozások - Valency vs Valence Electrons
A valency elektronok és a valence elektronok egymással összefüggő kifejezések, és a kulcskülönbség a valencia és a valence elektronok között. a valence elektronok az elemek legkülső héjában lévő elektronok míg valenciál elektronok az elektronok száma, amelyeket el kell fogadni vagy el kell távolítani a legközelebbi nemesgáz-konfiguráció eléréséhez. A legkülső héj elektronjai általában hozzájárulnak vegyi kötések kialakításához. Néhány atomban a valenceelektronok száma megegyezik a valence elektronok számával.
Mi a Valence elektron? Az atomok legkülső héjában lévő elektronok számát "valence-elektronoknak" hívják. Emiatt az atom legkülső héját "valence héjnak" hívják. Legtöbbször ezek az elektronok, amelyek részt vesznek a vegyi kötésben. Amikor az elemek kationokat képeznek, eltávolítják az elektronokat a valence héjból. Az elemben lévő valence-elektronok száma határozza meg a csoportot az időszakos táblában.

Az atomok legkülső héja feltöltéséhez vagy elvesztéséhez szükséges elektronok számát "valency electrons" -nak nevezzük. Egy adott atom esetében a valenciaelektronok száma függ az atomban lévő valenciaelektronok számától. A nátrium esetében a valencia értéke 1, mert eltávolítja az utolsó elektronot a legkülső héjban, hogy elérje a legközelebbi nemesgáz oktetszerkezetét.
|
Valence Electrons:
Az atomok legkülső shelljában lévő elektronokat "valence electrons" -nak nevezzük. Az "s" és a "p" csoportelemek esetében a valence elektronok száma megegyezik a csoportszámukkal.
Példa Valency Electrons:
Az elektronok számát, amelyeket el kell fogadni vagy el kell távolítani a legközelebbi nemesgenerátor elektronkonfigurációjának eléréséhez, az úgynevezett "valenciaelektronok" vagy egy atom "valenciája".
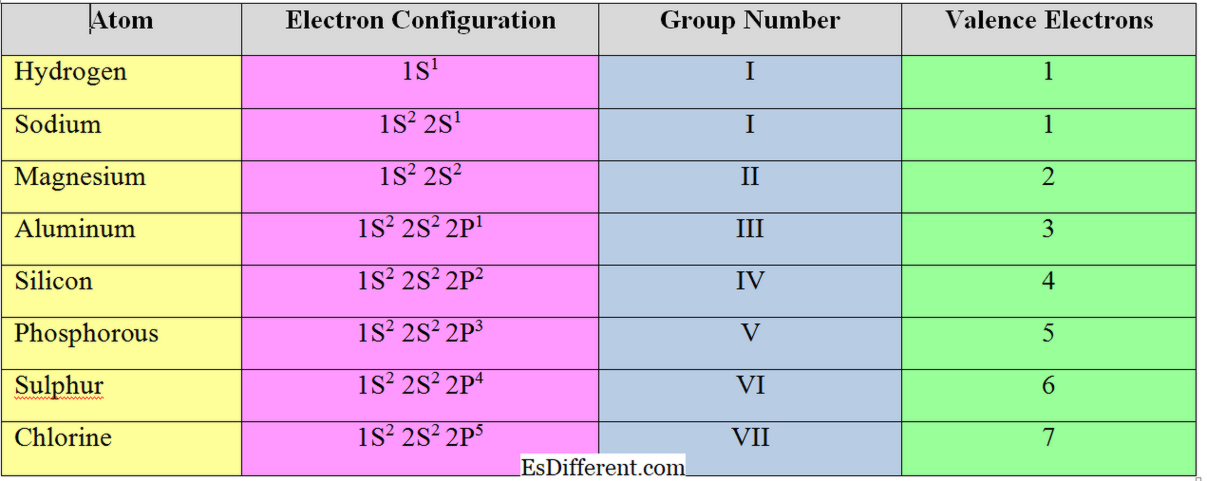
Általában a fém elemek (az I., II. És III. Csoportba tartozó elemek) esetében a valenceelektronok száma megegyezik a vegyérték elektronok számával; eltávolítják az elektront a valence héjban, hogy elérjék az oktet szerkezetét. De a nemfém elemek elfogadják az elektronokat, hogy elérjék a legközelebbi nemesgáz elektronkonfigurációját. Ezért a nemfém elemek valenciáját úgy számoljuk ki, hogy a teljes valenciál elektronokat kivonjuk 8-ból.
Klórhoz, Valenciál elektronok száma = 8-7 = 1
Valency és Valence Electrons
Valency és Valence VIII. Csoportba tartozó elemek elektronjai

Valence elektronok:
A VIII. Csoportba tartozó elemek nemesgázok, és kémiailag stabilak. A külső héja teljes, és nyolc elektronot tartalmaz a legkülső héjban (Helium -He kivételével); így a VIII. csoportba tartozó elektronok nyolc valence-elektront tartalmaznak.
Valency Electrons: Valency a más elemekkel vagy molekulákkal való kötődés képességének mértéke. A nemesgázok nem fogadják el vagy távolítják el az elektronokat, hogy elérjék az oktett szabályt, mivel már befejezték az utolsó héjat. Ezért a VII. Csoport elemeinek valenciája nulla.
Image Courtesy: "Electron shell 010 Neon - nincs címke" a commons: Felhasználó: Pumbaa (eredeti munka a közönség: Felhasználó: Greg Robson) - // commons. Wikimedia. org / wiki / Kategória: Electron_shell_diagrams (megfelelő címkézett verzió). (CC BY-SA 2. 0 uk) keresztül Commons




