Különbség az izotóniás és a hipertonikus | Izotóniás vs. hipertonikus
Kulcs különbség - Izotóniás vs. Hypertonic
Fontos megérteni a Tonicity koncepcióját, mielőtt az izotóniás és a hipertóniás különbséget elemezni fogjuk. Ezért először röviden írjuk le a tonicitás fogalmát és fontosságát. A tonicitás a két oldat vízkoncentrációjának változása, osztva féligáteresztő membránnal. Az oldatok viszonylagos vízkoncentrációja is megmagyarázható, amely meghatározza a víz diffúziójának irányát és mennyiségét, amíg a membrán mindkét oldalán egyenlő koncentrációt nem kap. A megoldások tónusának meghatározásával meghatározhatjuk, hogy a víz milyen irányú lesz. Ezt a jelenséget általában akkor alkalmazzuk, amikor bemutatjuk a külső oldatba merített sejtek reakcióját. Három osztályozás van a tonicitásnak, amelyet az egyik megoldás a másikhoz képest lehet. Hipertóniásak, hipotóniásak és izotóniásak. Az izotóniás és hipertóniás kulcs különbség , hogy a hipertóniás oldat több oldószert tartalmaz, mint az oldott anyagot , míg az oldott anyag és az oldószer egyenlő eloszlású az izotóniás oldatban. A hipertóniás és izotóniás megoldások megfogalmazása azonban nem lényeges, ha megértjük az izotóniás és a hipertóniás megoldások közötti különbséget.
Mi a hipertonikus?
A Hyper egy másik szó a fent vagy túlzott. A hypertonikus oldatoknak nagyobb a koncentrációja az oldott anyag (glükóz vagy só), mint a sejt. Az oldatok az oldószerben feloldott elemek, ezáltal megoldást képeznek. Egy hipertóniás oldatban az oldott anyagok koncentrációja nagyobb a sejten kívül, mint belül. Ha egy sejtet hipertóniás oldatba merítünk, akkor egy ozmotikus eltolódás következik be, és a vízből a vízmolekulák áramolnak ki az oldott anyagok koncentrációjának mérése és a sejt méretének zsugorodása között.
Mi az izotóniás?
Az Iso egy másik szó az egyenlőségért és a tonik a megoldás tonicitásához. Az izotóniás oldatok hasonló koncentrációjú oldott anyagokkal rendelkeznek, mint az a megoldás, amellyel összehasonlítjuk. Izotóniás oldatban az oldott anyagok koncentrációja azonos a sejten belül és kívül, ami egyensúlyt teremt a sejt szervezet környezetében. Amikor egy sejtet izotóniás oldatba merítenek, nem lesz ozmotikus eltolódás és a vízmolekulák diffundálnak a sejtmembránon keresztül mindkét irányban, hogy egyensúlyba hozzák az oldott anyagok koncentrációját.Ez a folyamat nem fog megdagadni vagy zsugorodni a cellában.

Mi a különbség az izotóniás és a hipertóniás között?
A hipertóniás és az izotóniás különbségek a következő kategóriákba sorolhatók.
A izotóniás és hipertóniás meghatározása
Hypertonic: "hiper" a fent említett vagy túlzott + "tonik" néven ismert, mint valami megoldás mentén. Így a hipertónia a megoldás fokozott tonicitását sugallja.
Izotóniás: "iso" ugyanazt a "+" tónust ismeri valami a megoldásvonal mentén. Így az izotóniás a megoldás hasonló tonicitását sugallja.
A izotóniás és hipertonikus
Az oldott anyag és az oldat koncentrációja
Hypertonic: Az oldat több oldószert tartalmaz, mint az oldott anyag.
Izotóniás: Az oldatban lévő oldószer és oldószer egyenlő eloszlású.
Példák
Hypertonic: Tisztított víz, mivel a tisztított vízben nem / kevésbé oldódik fel, és koncentrációja nagyon alacsony a sejtes környezethez képest.
izotóniás: sóoldat izotóniás humán vérplazmára
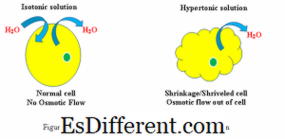
sejtek reakciója hipertóniás és izotóniás oldatban (lásd az 1. ábrát)
hipertóniás: hipertóniás környezetben a víz a sejtmembránon keresztül áramlik ki a sejtből, annak érdekében, hogy egyensúlyban legyen az oldott anyagok koncentrációja mind a sejtben, mind a sejt környezetében. Ennek eredményeképpen a cella zsugorodik , mivel a víz elhagyja a cellát, hogy csökkentse az oldott anyag koncentrációját a külső környezetben.
Izotóniás: Ha egy sejt izotóniás oldatban van, akkor nem okoz duzzanatot vagy zsugorodást.
Vízkoncentráció gradiens
Hypertonic: Vízkoncentráció gradiens figyelhető meg a sejt belsejéből a hipertóniás oldathoz
Izotóniás: Vízkoncentráció gradiens nem létezik
Oldott koncentráció gradiens < Hypertonic:
A sejtkoncentráció gradiens a hypertonikus oldatból a sejt belsejébe nézve Izotóniás:
Az oldott koncentráció gradiens nem létezik. Osmotikus elmozdulás
Hypertonic:
ozmotikus eltolódás létezik. Izotóniás:
ozmotikus eltolódás nem létezik Víz mozgása
Hypertonic:
A vízmolekulák gyorsan mozognak vagy diffundálnak a sejt belsejéből a külső oldat irányába, így a sejt elveszíti a vizet. Izotóniás:
A vízmolekulák mindkét irányba mozognak vagy diffúzálódnak, és a víz diffúzió sebessége mindkét irányban hasonló. Tehát a sejt vagy vizet nyer vagy veszít. Sportitalok
Izotóniás:
Az izotóniás ital hasonló koncentrációjú sót, cukros szénhidrátot és elektrolitokat tartalmaz, mint az emberi testben. Az izotóniás sport italt gyakran előnyösek orális rehidratációs oldatként. Általában 4-8 g szénhidrátot tartalmaz 100 ml-enként. Hypertonic:
A hypertonikus ital magasabb koncentrációjú sót, cukros szénhidrátot és elektrolitokat tartalmaz, mint az emberi testben.Általában körülbelül 8 g szénhidrát / 100 ml. Az ozmoterápiában hipertóniás megoldást is alkalmaznak agyi vérzés kezelésére. A hipertóniás sportitalok ideálisak azok számára, akiknek nagyon nagy energiát igényelnek. Összefoglalva, három megoldás létezik, amelyek az oldott koncentráción alapulnak, és izotóniásak, hipotóniásak és hipertóniak. Az oldott anyagok koncentrációja ugyanolyan, mint a sejten belül és kívül egy izotóniás oldatban. Az oldott anyagok koncentrációja nagyobb a sejten belül, mint a külső környezet hipotóniás oldatban, míg a hipertóniás oldat olyan, ahol az oldott anyagok koncentrációja nagyobb a környezettel szemben, mint a belső sejt.
Referenciák Mansoor, M. A., Beverly, J., és Sandmann. (2002). Alkalmazott fizikai gyógyszertár. McGraw-Hill Professional. 54-57. Voet, D., Judith, G. V. és Charlotte, W. P. (2001). Biokémiai alapismeretek (Rev. szerk.). New York: Wiley. o. 30. Képesség: A LadyofHats által "Osmotic pressure on blood cells diagram" - a magam [1], [2], [3] és [4] … (Public Domain) alapul a Wikimedia Commons




