Különbség Pyruvate és Pyruvic Acid között | Pyruvate vs Pyruvic Acid
Kulcskülönbség - Pyruvate vs Pyruvic Acid
A piruvát és a piroszőlős savak gyakran felcserélhetőek; Mindazonáltal különbség van közöttük:
A piroszőlősav sav, ami azt jelzi, hogy képes hidrogéniont felszabadítani és kötni egy pozitív töltésű nátrium- vagy káliumionnal annak érdekében, hogy savas sót képez, amelyet piruvátnak is neveznek. Más szavakkal, piruvát egy piruvinsav sója vagy észtere. Ez a kulcskülönbség a piruvát és a piroszőlősav között, és mindkét anyagot biológiai és anyagcsere útjaiban alkalmazzák, de szorosan összekapcsolódnak.
Mi a Pyruvic Acid?A piroszőlősav jelentős szerepet játszik az emberi anyagcserében. Például az élő sejteket sejtenergiával aerob légzéssel biztosítják, vagy piruvássav fermentálódik fermentáció útján tejsav előállításához. A piros sav folyékony a természetben, színtelen és az ecetsavhoz hasonló illatú. Gyenge sav, és vízben oldódik. A piruvinsav kémiai képlete (CH
3 COCOOH), és az alfa-keto-savak legegyszerűbb formájának tekinthető egy karbonsavval és egy keton funkciós csoporttal. Ezenkívül a piruvinsav egy karbonsav, amely nem olyan erős, mint a szervetlen savak, például a sósav.

Pyruvate a piroszőlősav konjugált bázisa, kémiai képlete CH3COCOO
- . Más szavakkal, a piruvát a piroszőlősavból előállított anion. A piruvinsav és a piruvát közötti legfontosabb különbség az, hogy a karbonsavcsoporton lévő hidrogénatom disszociált, vagy eltávolították. Ez negatív töltésű karboxilátcsoportot biztosít a piruvátnak. A piruvinsav gyenge savasságának köszönhetően könnyen elválik vízben, és így piruvátot képez. A piruvát fontos kémiai vegyület az emberi anyagcserében és biokémiában. A piruvát a glükóz metabolizmusában vesz részt, és glikolízisként is ismert. A glikolízis folyamatban egy molekula glükózt bontanak le két molekula piruvátra, amelyeket ezután további reakciókban alkalmaznak az energia előállítására.
A piruvát és a piroszőlősav lényegesen eltérő kémiai hatásokkal és néhány funkcionális tulajdonsággal rendelkezik. Ezeket a különbségeket itt tárgyaljuk.
A
Pyruvate és Pyruvic Acid meghatározása Pyruvic acid: Pyruvic acid
sárgás szín szerves sav . Pyruvate: Pyruvate egy piroszőlősav sója vagy észtere.
Pyruvate and Pyruvic Acid Chemical Formula and Molecular Structure
Pyruvic acid : CH
3
COCOOH Pyruvate : CH3COCOO -
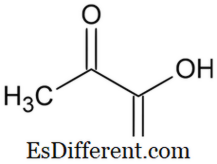
Proton és Electron Balance Pyruvic acid: A piruvavasavnak
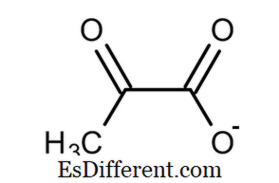
azonos számú elektronja van, mint a protonok
. Pyruvate: A piruvátnak több elektronja van, mint a protonok
. Synthesis Pyruvic acid: Pyruvic acid szintetizálható tejsavból.
Pyruvate:
Pyruvate a piroszőlősavból szintetizált anion. Amikor a piruvasav feloldódik vízben, hajlamos disszociálni és szintetizálni egy piruvát iont és egy protonot. Savasság
Pyruvic acid: Pyruvic acid egy gyenge szerves sav.
Pyruvate:
Pyruvate a piroszőlősav konjugátum alapja. Karboksilfunkcionális csoport
Piruvinsav: A piruvinsav karbonsav (COOH) funkciós csoportot tartalmaz.
Pyruvate:
A piruvátot karboxilát anionnak nevezik, amely COO -.
Töltés Pyruvic acid: Pyruvic acid
semleges töltés
. Pyruvate: Pyruvate negatív töltés
. Proton beadása Pyruvic acid: Pyruvic acid képes proton feladására.
Pyruvate:
A piruvát nem adhat fel protonot. Domináns forma
Pyruvic acid: A piruvavasav
kevésbé domináns
formában van sejtes környezetben a piruváthoz képest. Pyruvate: Pyruvate a több
domináns forma celluláris környezetben a piruvinsavhoz képest. Intra-molekuláris Hydrogen Bond Pyruvic acid:
A piruvavasav intra-molekuláris hidrogénkötés van. Pyruvate:
A piruvátnak nincs intra-molekuláris hidrogénkötése. Referenciák:
Cody, G. D., Boctor, N. Z., Filley, T. R., Hazen, R. M., Scott, J.H., Sharma, A. és Yoder, H. S. (2000). Primordiális karbonilezett vas-kénvegyületek és a piruvát szintézise. Science, 289
(5483): 1337-1340.
Kép jóvoltából: "Pyruvic-acid-3D-balls". (Public Domain) a Wikimedia Commons segítségével.




