Különbség a lizin és az L-lizin között | Lizin vs. L-lizin
Kulcs különbség - Lizin vs L-lizin
A lizin és az L-lizin mindkét típusú aminosav, ugyanazokkal a fizikai tulajdonságokkal rendelkeznek némi különbség van közöttük. A kulcs különbség a lizin és az L-lizin között képes a sík polarizált fény elforgatására. A lizin biológiailag aktív, természetben előforduló esszenciális α-aminosav. Két izomer alakban fordulhat elő, mivel két különböző enantiomer képződik a királis szénatom körül. Ezek L- és D- formákként ismertek, hasonlóan a balkezes és jobbkezes konfigurációkhoz. Ezek az L- és D- formák optikailag aktívak, és a sík polarizált fényt más értelemben forgatják; jobbra vagy balra. Ha a fény az óramutató járásával ellenkező irányban forgatja a lizint, akkor a fény levorotációt mutat, és L-lizineként ismert. Mindazonáltal gondosan meg kell jegyeznünk, hogy az izomerek D- és L-jelölése nem egyezik meg a d- és l-jelöléssel.
Mi a lizin?
A lizin esszenciális aminosav , amely nem szintetizált a szervezetünkben , és azt a rendszeres étrendnek kell biztosítania. Ezért a lizin egy esszenciális aminosav az ember számára. Ez egy biológiailag fontos szerves vegyület, amin amin (-NH 2 ) és karbonsav (-COOH) funkcionális csoportok NH 2 (CH 2) 4 -CH (NH 2 ) - COOH. A lizin legfontosabb elemei a szén, a hidrogén, az oxigén és a nitrogén. A biokémiában az első (alfa) szénatomhoz mind az amin, mind a karbonsavcsoportok aminosavai ismertek, mint a-aminosavak . Így a lizint is a-aminosavaknak tekintjük. A lizin szerkezete az 1. ábrán látható. 1. ábra: A lizin molekuláris szerkezete (* a szénatom egy királis vagy aszimmetrikus szénatom és az alfa-szénatom is)
A lizin bázikus jellegű, mert két bázikus amino- csoportok és egy savas karbonsavcsoport. Ezért két aminocsoport jelenléte miatt is kiterjedt hidrogénkötést képez.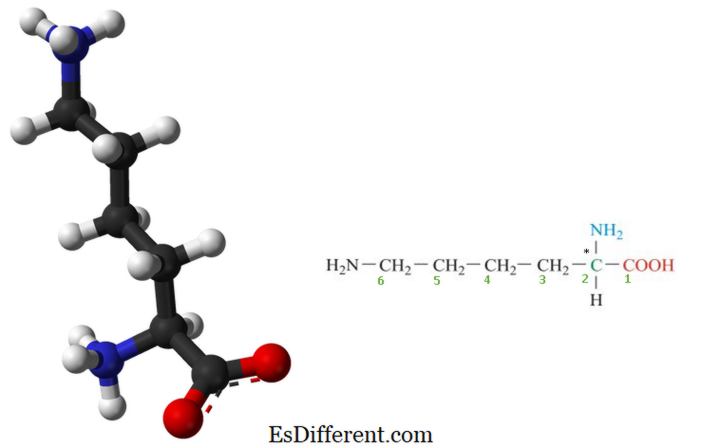
A jó lizinforrások
fehérje gazdag állati eredetűek, például tojás, vörös hús, bárány, sertés, baromfi, sajt és bizonyos halak (mint a tőkehal és a szardínia). A lizin is növényi fehérjékben gazdag mint a szója, a bab és a borsó. Azonban ez a korlátozó aminosav a legtöbb gabonamagban, de bővelkedik a legtöbb pulzusban és hüvelyben.
nd
szén körül, és aszimmetrikus szerkezet .Ezenkívül a lizin egy optikailag aktív aminosav, ennek az aszimmetrikus vagy királis szénatomnak a jelenlétében. Így a lizin sztereoizomereket hozhat létre, amelyek ugyanolyan molekulatömegű izomer molekulák, de térben térnek el az atomjuk háromdimenziós orientációiban. Az enantiomerek két sztereoizomerek, amelyek egymáshoz viszonyítva visszaverődéssel kapcsolódnak egymáshoz, vagy egymás tükörképei, amelyek nem egymásra helyezhetők. A lizin két enantiomer formában áll rendelkezésre, az L- és D-, és a lizin enantiomerjei a 2. ábrán láthatók. 2. ábra: Lizin aminosav enantiomerjei. A COOH, H, R és NH2 csoportok az óramutató járásával megegyező módon a C atom körül vannak elrendezve, az enantiomert L-formának és D-formának nevezzük. L- és D- csak a szénatom körüli térbeli elrendezésre utalnak, és nem utalnak az optikai aktivitásra. Miközben a királis molekula L- és D- formái a polarizált fény síkját különböző irányban forgatják, egyes L-alakok (vagy D-alakok) balra forgatnak (levo vagy l-forma), és néhányat jobbra (dextróz vagy d-forma). Az l- és d- formákat optikai izomereknek nevezzük. Az L-lizin és a D-lizin egymásnak enantiomerjei azonos fizikai tulajdonságokkal rendelkeznek, kivéve az irányt, amelyben polarizált fényt forgatnak. Nem egymásra helyezhető tükörképviszonyuk van. Ugyanakkor a D és L nómenklatúrája nem gyakori az aminosavakban, beleértve a lizint. A sík-polarizált fényt ugyanolyan nagyságú, de különböző irányban forgatják. A lizin D és L izomerjét, amely a sík polarizált fényt az óramutató járásával megegyező irányba forog, jobbra forgó vagy

d-lizin
-nak nevezik, és az az, amelyik forgatja a sík polarizált fényt az óramutató járásával ellentétes irányba, L-lizin (2. ábra). Az L-lizin a a legtöbb rendelkezésre álló lizinforma
. A D-Lizin a lizin szintetikus formája, és az l-lizinből racemizálással szintetizálható. Ezt a poli-d-lizin feldolgozásánál alkalmazzák, amelyet bevonóanyagként használnak a sejtek kötődésének fokozására. Az L-lizin jelentős szerepet játszik az emberi szervezetben, a kalcium felszívódásában, az izomfehérjék fejlődésében és a hormonok, enzimek és antitestek szintézisében. Ipari módon az L-lizint mikrobiális erjesztési eljárással állítják elő, Corynebacterium glutamicum -ot alkalmazva. Mi a különbség a lizin és az L-lizin között? A lizin és az L-lizin ugyanazokkal a fizikai tulajdonságokkal rendelkezik, kivéve az irányt, amelyben polarizált fényt forgatnak. Ennek eredményeként az L-lizinek lényegesen eltérő biológiai hatásai és funkcionális tulajdonságai lehetnek. Nagyon korlátozott kutatást végeztek azért, hogy megkülönböztessék ezeket a biológiai hatásokat és funkcionális tulajdonságokat. Néhány ilyen különbség lehet:
Íz
L-lizin:
Az aminosavak L-formái általában íztelenek.
D-lizin: Az aminosavak D-formái általában édes ízűek.
Ezért az l-lizin kevesebb lehet / nem édesebb, mint a lizin. Abundancia
L-lizin:
Az aminosav l-formái, beleértve az l-lizint, a természetben a legelterjedtebb forma.Például a proteinekben általánosan megtalálható tizenkilenc L-aminosav közül kilencek jobbra forgatnak, a fennmaradó rész pedig balra forgó.
D-lizin: A kísérletileg megfigyelt aminosavak D-formái nagyon ritkán fordultak elő.
Referenciák: Solomons, T. W. Graham és Graig B. Fryhle (2004). Organic Chemistry (8 th
ed). Hoboken: John Wiley & Sons, Inc. Everhardus, A. (1984). Sztereokémiája, amely alapja a kifinomult ostobaságnak a farmakokinetikában és a klinikai farmakológiában, European Journal of Clinical Pharmacology, 26, 663-668. Image Courtesy: "Ben-Mills" L-lizin monokion-a-hidroklorid-dihidrát-xtal-3D-golyó "- Saját munka a Wikimedia Commons-ban



